Gesundheit heute
Kleines Lexikon der Leukämietherapie
Agranulozytose: Absinken der Granulozyten unter 500 pro µl Blut. Dadurch extreme Infektionsgefahr und Notwendigkeit weit reichender Vorsichtsmaßnahmen (siehe Knochenmarktransplantation).
Klassifizierung des Therapieerfolgs
- Remission: Tumorrückbildung
- Teilremission: Deutliche Tumorrückbildung (über die Hälfte). Bei Leukämie weniger als 25 % Leukämiezellen im Blut, weniger als 5 % im Knochenmark
- Vollremission: Kein Tumor mehr nachweisbar. Bei Leukämie Normalisierung des Blutbilds, weniger als 5 % Leukämiezellen im Knochenmark
- Minimale Resterkrankung (minimal residual disease): Nachweis von Leukämiezellen mit molekulargenetischen Methoden, nicht aber mit konventionellen Diagnoseverfahren wie etwa der Mikroskopie. Zunehmende Bedeutung in der Prognoseabschätzung und der Behandlungsplanung nach erreichter Vollremission
Immunphänotypisierung und Monoklonale Antikörper
CD-Moleküle. Wie alle Körperzellen sind auch die weißen Blutkörperchen von einer Zellmembran umschlossen. Auf ihrer Oberfläche befinden sich verschiedene Eiweiße, die CD-Moleküle, die wahrscheinlich für die Kommunikation der Abwehrzellen eine Rolle spielen. Sie werden auch für die exakte Klassifikation einer Leukämie herangezogen, denn welche der über 200 CD-Moleküle ein weißes Blutkörperchen auf seiner Oberfläche trägt, hängt von seiner genauen Art und seiner Entwicklungsstufe ab. So trägt etwa ein B-Lymphozyt die Moleküle CD19–CD21 auf seiner Zellmembran, ein T-Lymphozyt hingegen die Moleküle CD2, CD3, CD5, CD7 und je nach Untergruppe CD4 (T-Helferzelle) oder CD8 (zytotoxische T-Zelle).
Monoklonale Antikörper. Mithilfe gentechnisch hergestellter monoklonaler Antikörper, die alle genau gleich sind und ganz exakt jeweils nur zu einem CD-Molekül passen, können Leukämien heute viel genauer differenziert und eingeteilt werden als noch vor wenigen Jahren. Richtig interessant wird diese Immunzytologie oder Immunphänotypisierung aber erst durch ihre Konsequenzen für die Behandlung:
Zum einen können Leukämien, deren Zellen unter dem Mikroskop gleich aussehen, sich aber durch die CD-Moleküle auf den Membranen unterscheiden, ganz unterschiedlich auf die „konventionelle“ Leukämiebehandlung ansprechen.
Zum anderen können auch die monoklonalen Antikörper selbst zur Behandlung genutzt werden. Sie entfalten ihre Wirkung entweder, indem sie die normale Signalwirkung des Moleküls blockieren, oder es werden im Vorfeld Gifte oder radioaktive Substanzen labortechnisch an sie gebunden, wodurch die kranken Zellen genauer getroffen werden als bei den bislang gängigen Therapien.
Beispiele für heute schon genutzte monoklonale Antikörperpräparate (MABs) sind Alemtuzumab (MabCampath®, gegen CD52), Rituximab (MabThera®, gegen CD20) oder Gemtuzumab (gegen CD33, in Mylotarg® gekoppelt an ein Zellgift). Selbst wenn die Therapieergebnisse mit den monoklonalen Antikörpern alles in allem ermutigend sind – insgesamt steckt diese Behandlungsform der Leukämie noch in den Kinderschuhen, und manch neue Therapieform konnte die in sie gesetzten Hoffnungen letztendlich nicht erfüllen.
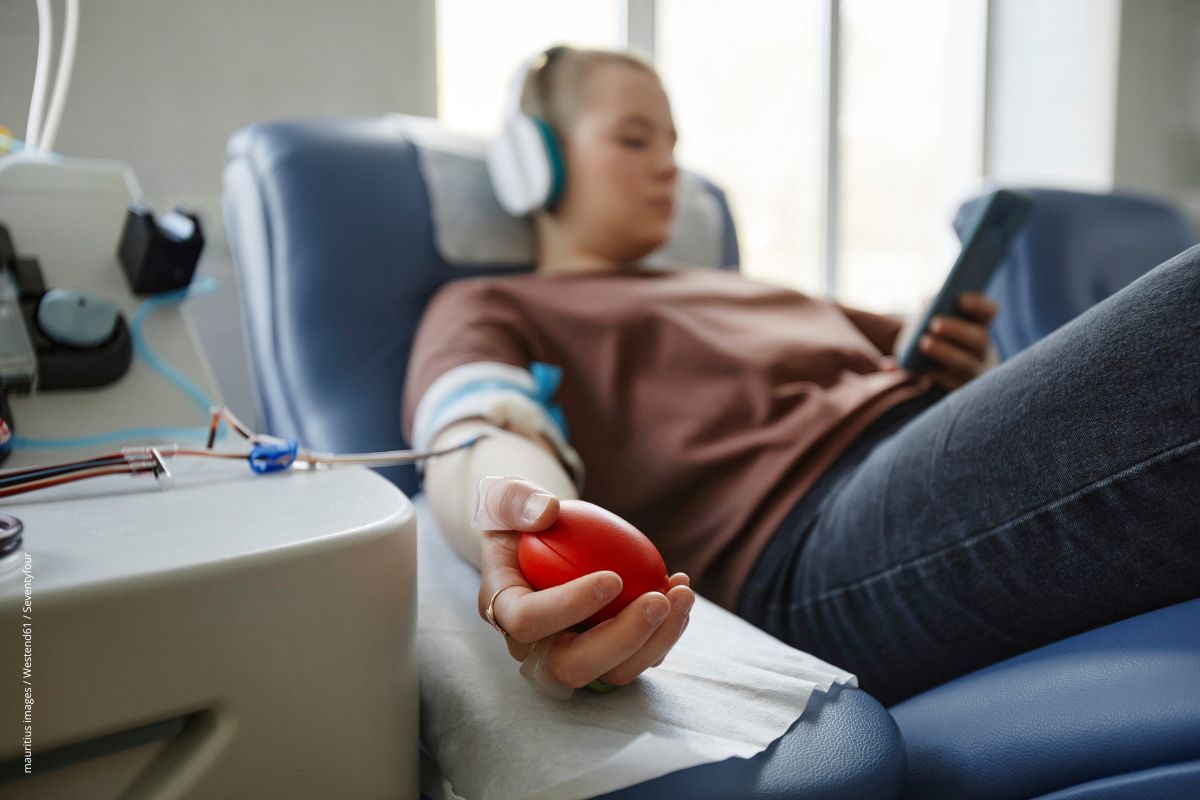
Regelmäßige Blutspenden regen das Knochenmark an und sollen vor Blutkrebs schützen.
Blutspenden als Schutz vor Blutkrebs?
Gesunde Reaktion
Wer Blut spendet, tut nicht nur etwas Gutes für die Allgemeinheit: Möglicherweise schützen regelmäßige Blutspenden auch vor Krebs.
Blutproduktion auf Hochtouren
Wenn der Körper Blut verliert, läuft die Produktion neuer Blutzellen im Knochenmark auf Hochtouren. Das geschieht auch bei regelmäßigen Blutspenden. Theoretisch könnte durch die starke Aktivierung der Stammzellen im Knochenmark die Mutation zu bösartigen Zellen gefördert werden – also die Gefahr für Blutkrebs (Leukämie) ansteigen. Dass womöglich das Gegenteil der Fall ist, konnte eine Gruppe von Forschenden jetzt zeigen.
Unterschiedliche Mutationen
Sie verglichen die Blutproben von 219 älteren Männern, die in ihrem Leben mehr als 100 Mal Blut gespendet hatten mit denen von 217 Männern und Frauen, die dies im gleichen Zeitraum nur bis zu 10 Mal getan hatten. Die genetische Vielfalt der Blutzellen war in beiden Gruppen gleich groß. Das bedeutet, dass die im Alters zunehmenden Veränderungen am Erbgut etwa gleich häufig waren. Unterschiede zeigten sich jedoch, wo diese Mutationen auftraten.
Bei den Vielspendern zeigten sich die Mutationen insbesondere an den Regionen des Erbguts, die bekanntermaßen keinen Blutkrebs begünstigen. Bei den anderen Studienteilnehmenden waren dagegen riskante, präleukämische Veränderungen häufiger.
Vorzeichen für Blutkrebs
Das unterstrich auch der Tierversuch: Es zeigte sich, dass die in Mäuse injizierten Stammzellen der Vielspender das Wachstum normaler gesunder roter Blutkörperchen förderten. Die Zellen der Wenigspender*innen, also die Zellen mit präleukämischen Veränderungen, lösten dagegen einen deutlichen Anstieg weißer Blutkörperchen aus. Das wird als mögliches Vorzeichen für Blutkrebs interpretiert.
Diesen Versuchen zufolge führt die Reaktion auf häufige Blutspenden nicht zu bösartigen Mutationen in den Stammzellen, sondern zu einer gesunden Blutproduktion. Regelmäßiges Blutspenden könnte dadurch vor Blutkrebs schützen, mutmaßen die Forscher*innen.
Quelle: Blood

